
- Autorius Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Paskutinį kartą keistas 2025-01-22 17:04.
Jei kreivė eina pagal laikrodžio rodyklę, konfigūracija yra R; jei kreivė eina prieš laikrodžio rodyklę, konfigūracija yra S. Norėdami gauti keturių skaičių prioritetinį pakaitalą viršuje Fišerio projekcija , turite naudoti vieną iš dviejų leidžiamų judesių, pavaizduotų antrajame paveikslėlyje.
Taip pat kyla klausimas, kaip priskirti R ir S konfigūraciją?
Kai visi jūsų pakaitalai buvo tinkamai suskirstyti pagal prioritetus, dabar galite pavadinti / pažymėti molekulę R arba S . Įdėkite žemiausio prioriteto pakaitalą atgal (punktyrinė linija). Nustatykite, ar kryptis nuo 1 iki 2 iki 3 pagal laikrodžio rodyklę ar prieš laikrodžio rodyklę.
Taip pat galima paklausti, kaip nustatyti, ar Fišerio projekcija yra chiralinė? Norėdami pagaminti a Fišerio projekcija , žiūrite a chiralinis centre, kad du pakaitai išeitų iš plokštumos pas jus, o du pakaitai grįžtų į plokštumą, kaip parodyta čia. Tada chiralinis centras tampa kryžiumi ant Fišerio projekcija . Kiekvienas kryžius ant a Fišerio projekcija yra chiralinis centras.
Panašiai, kaip pereiti nuo Fišerio projekcijos prie obligacijos linijos?
Norėdami konvertuoti Fišerio projekcija į a obligacijų linija formulę tiesiog nupiešite zigzagą linija šešių anglies atomų. Tada įdėkite aldehido grupę prie C-1 ir OH grupių ant kiekvienos iš kitų penkių anglies atomų. Atkreipkite dėmesį, kad obligacijų linija formulė nesuteikia stereocheminės informacijos.
Kuo skiriasi enantiomerai ir diastereomerai?
Yra dviejų tipų stereoizomerai: enantiomerai ir diastereomerai . Enantiomerai turėti chiralinis centrai, kurie yra veidrodiniai atvaizdai ir kurių negalima uždėti. Diastereomerai turėti chiralinis centrai, kurie nėra uždedami, bet NĖRA veidrodiniai vaizdai. Priklausomai nuo stereocentrų skaičiaus, jų gali būti daug daugiau nei 2.
Rekomenduojamas:
Kaip elektronų konfigūracija susijusi su kvantiniais skaičiais?
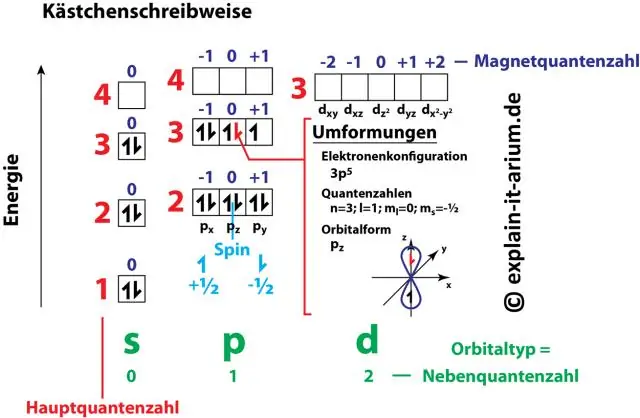
Skaičių ir raidžių poros elektronų konfigūracijoje reiškia du iš keturių elektrono kvantinių skaičių. Šie kvantiniai skaičiai mums suteikia daugiau informacijos apie elektronų ir jų orbitų savybes. Pagrindinis kvantinis skaičius (n) nurodo elektrono energijos lygį ir jo dydį
Kaip rašote MN elektronų konfigūraciją?

Kita vertus, mangano elektronų konfigūracija yra 1s22s22p63s23p64s23d5 ir inertinių dujų konfigūracija [Ar] 4s23d5, todėl kiekvienoje 3d suborbitoje yra vienas nesuporuotas elektronas
Kaip žinoti, ar jo R ar S konfigūracija?

Kadangi 4-as didžiausio prioriteto atomas yra užpakalinėje dalyje, rodyklė turėtų atrodyti taip, lyg ji eitų per laikrodžio ciferblatą. Jei jis eina pagal laikrodžio rodyklę, tai yra R-enantiomeras; Jei jis eina prieš laikrodžio rodyklę, tai yra S-enantiomeras
Kaip rasti deguonies elektronų konfigūraciją?

Rašant deguonies elektronų konfigūraciją, pirmieji du elektronai eis 1s orbitale. Kadangi 1s gali laikyti tik du elektronus, kiti 2 elektronai O eina 2s orbitoje. Likę keturi elektronai eis 2p orbitale. Todėl O elektronų konfigūracija bus 1s22s22p4
Kaip žingsnis po žingsnio atliekate elektronų konfigūraciją?

Veiksmai Raskite savo atomo atominį skaičių. Nustatykite atomo krūvį. Prisiminkite pagrindinį orbitų sąrašą. Suprasti elektronų konfigūracijos žymėjimą. Įsiminkite orbitų tvarką. Užpildykite orbitales pagal elektronų skaičių jūsų atome. Naudokite periodinę lentelę kaip vaizdinį nuorodą
